http://ceippedropenzollab.blogspot.com.es/2015/11/cristalizacion-de-la-sal-comun.html
http://fcayqca.blogspot.com.es/2014/01/nacl-sal-comun_26.html
"Trata a los demás como quieras que te traten a tí"
jueves, 27 de octubre de 2016
miércoles, 26 de octubre de 2016
BLOQUE 2: el ruido
1_ ¿que es una onda? ¿tipos de ondas?
https://www.youtube.com/user/jasalamero
https://www.youtube.com/user/jasalamero
- mas información sobre Tipos de onda
- Después de ver estos vídeos realiza las siguientes actividades que encuentras en el siguiente enlace:
martes, 25 de octubre de 2016
martes, 18 de octubre de 2016
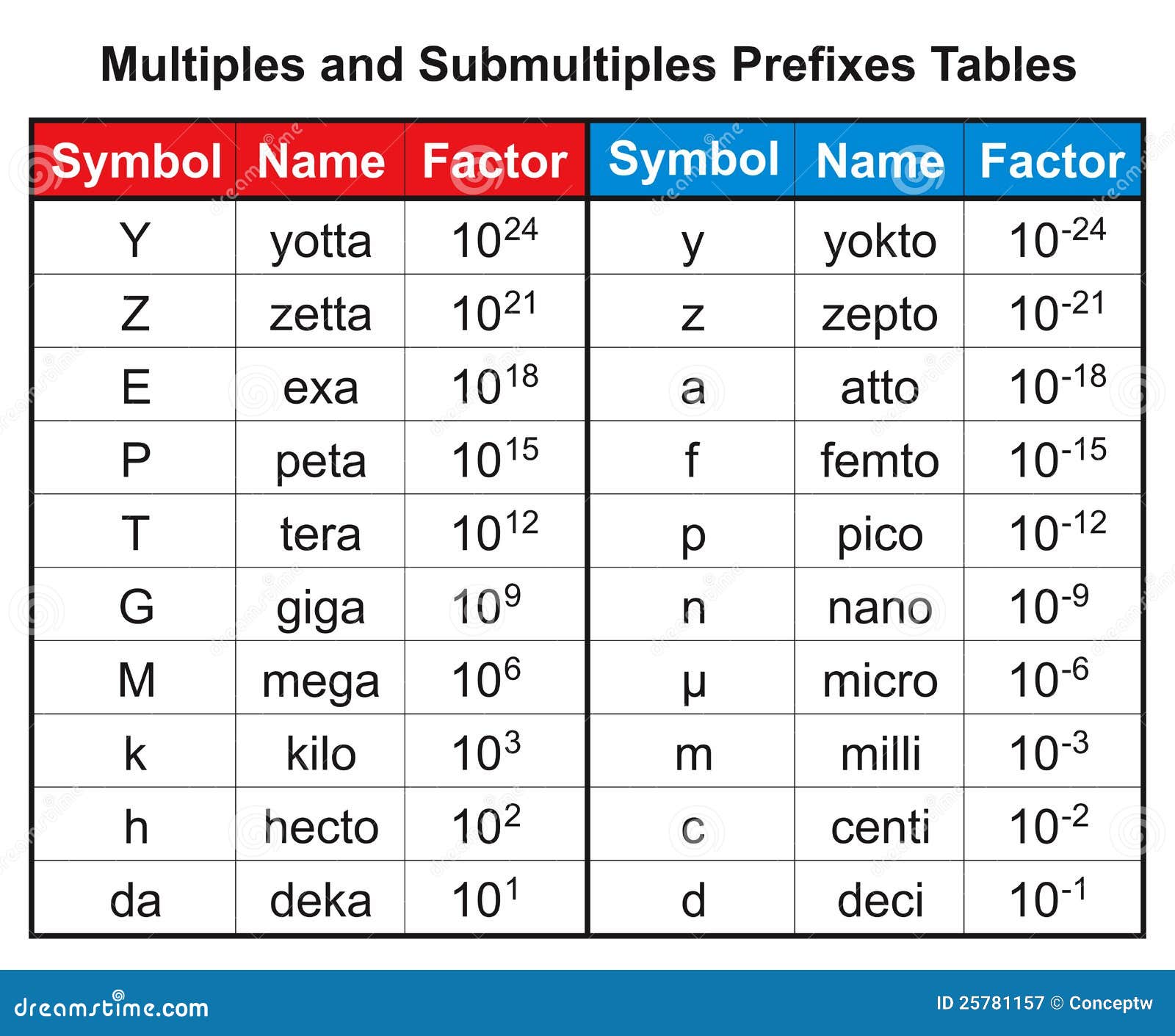
Algunas unidades que con frecuencia aparecen en temas de higiene laboral y
están relacionadas con los agentes químicos son:
p.p.m. Partes por millón expresadas volumétricamente y medidas a 25ºC y 760 mm Hg.
p.p.b. Partes por billón (billón americano = 109) = 10-3 p.p.m.
mg/m3 Miligramos por metro cúbico. Expresa la concentración en forma gravimétrica.
m.p.p.m3 Millones de partículas por metro cúbico.
m.p.p.c.f. Millones de partículas por pie cúbico.
p.p.c.c. Partículas por centímetro cúbico.
nm Nanómetro, milmillonésima parte del metro = 10-9 m.
μm
Micrómetro, millonésima parte del metro = 10-6 m.
μg Microgramo, millonésima parte del gramo = 10-6
g.
μl Microlitro, millonésima parte del litro = 10-6 l
mg Miligramo =10-3 g.
ml Mililitro = 1 cm3 = 10-3 l.
m3 Metro cúbico = 103 l = 103 dm3.
atm Atmósfera = 760 mm Hg = 760 torr = 1,01325.105 Pa (≡N/m2) = 1,01325 bar.
jueves, 13 de octubre de 2016
jueves, 6 de octubre de 2016
¿Qué son las partes por millón (ppm)?
¿Qué son las partes por millón (ppm)?: Las partes por millón, y en general “partes por notación“, es una pseudo unidad medida que se utiliza para describir fenómenos de relación como “partes de un todo”, por ejemplo concentraciones. En concreto, una ppm representa 1 parte de un 1 millón, esto es 1/1000000 o 1×10-6:


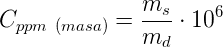

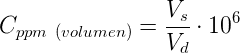



- Es similar al concepto de porcentaje. El 1% sería una parte de 100 (102) mientras que 1 ppm sería un aparte de 106. La equivalencia entre porcentaje y ppm es la siguiente:
O
Ejemplos de uso: medida de concentraciones
El uso más habitual de ppm es en análisis químico para la medida de concentraciones muy diluidas.
- ppm en masa/masa
La concentración en partes por millón expresada en masa/masa se calcula dividiendo la masa del soluto (ms) entre la masa de la disolución (md, suma de la masa del soluto y la masa del disolvente), ambas expresadas en la misma unidad y multiplicadas por 106 (1 millón). Se suele nombrar como ppmm:
Por ejemplo, podemos expresar ambas masas en gramos. Si a 1500 g de agua le añadimos 0.01 g de un soluto:
Cppm = ( 0.01 / 1500.01 ) × 106 = 6.66 ppmm
Por tanto, una disolución de 0.01 g en 1500 g de disolvente tiene una concentración de 6.67 ppm. En el SI sería equivalente a una concentración de 6.66 mg/kg (1 ppm = 1 mg/kg).
Cómo la mayoría de las veces que se utilizan las partes por millón el soluto está muy diluido, es común que se desprecie en el denominador y simplemente se divida la masa del soluto entre la masa del disolvente.
Si no conocemos la masa de disolvente pero conocemos su volumen y su densidad, se puede calcular la masa como el volumen por la densidad, ya que la densidad (ρ, kg/m3 en el SI) es:
Recuerda que si el disolvente es agua, la densidad es prácticamente igual a 1 kg/L, lo que quiere decir que 1 L de agua tiene una masa aproximadamente igual 1 kg. Por tanto, si 1 ppm = mg/kg, en el caso del agua sería equivalente 1 mg/L.
- ppm en volumen/volumen
La expresión de una concentración en partes por millón volumen-volumen es similar a la expresión masa-masa. Se obtiene dividiendo el volumen de soluto (Vs) entre el el volumen de la disolución (Vd, volumen del soluto más el volumen del disolvente) y se multiplica por 106. Se suele nombrar como ppmv:
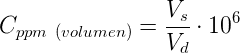
Por ejemplo, si disolvemos 1 ml de acetona en 2 L de agua (2 L = 2000 ml):
C(volumen/volumen) = ( 1 / 2001 ) x 106 = 499.75 ppmv
En el Sistema Internacional de Unidades sería equivalente a 499.75 μl/L (1 ppm = 1 μl/L), ya que un μl es una millonésima parte de 1 L.
Uno de los ejemplos más comunes del uso de partes por millón en volumen/volumen es paramedir concentraciones en el aire. Por ejemplo, en esta noticia se puede leer como la concentración media de CO2 en la atmósfera terrestre superó las 400 ppm. Esto quiere decir que cada litro de aire contiene 400 μl de CO2, o lo que es lo mismo, que el 0.04 % de la atmósfera es CO2 (recuerda que 1 ppm = 0.0001 %).
- ppm en masa/volumen
Muchas veces la concentración se expresa como masa de soluto en un determinado volumen de disolución. Las partes por millón en masa/volumen se calculan dividiendo la masa del soluto en gramos entre el volumen de disolución en mililitros y se multiplica por 106:

Qué sería equivalente a la masa del soluto en mg entre el volumen en litros:

En el caso del agua, o cualquier otro disolvente de densidad igual a 1 kg/L, sabemos que 1 kg tiene un volumen de 1 L. Para otros disolventes podemos obtener su volumen en litros si conocemos su masa y densidad. Por ejemplo, tenemos 0.5 mg de soluto y 0.2 kg de un disolvente de densidad de 0.95 kg/L. El volumen en litros del disolvente sería:
V = 0.2 / 0.95 = 0.21 L
Y la concentración en ppm masa/volumen sería:
C (masa/volumen) = 0.5 / 0.21 = 2.38 ppm
Relación con otras partes por notación
| Nombre | Notación | Coeficiente |
|---|---|---|
| Por ciento | % | 10-2 |
| Por mil | ‰ | 10-3 |
| Partes por millón | ppm | 10-6 |
| Partes por billón | ppb | 10-9 |
| Partes por trillón | ppt | 10-12 |
- cuando trabajamos con los valores de los contaminantes en agua o en aire, condisoluciones de muy bajas concentraciones o con la cantidad de partículas de polvo en un ambiente, entre otros.

miércoles, 5 de octubre de 2016
Solubilidad en agua (A6)
NTP 663: Propiedades fisicoquímicas relevantes en la prevención del riesgo químico
- El objetivo de esta Nota Técnica de Prevención es proporcionar a los profesionales que están expuestos a productos químicos a consecuencia de su trabajo, una serie de criterios que les permitan interpretar de forma práctica los datos fisicoquímicos que figuran en las Fichas de Datos de Seguridad (FDS) suministradas con el producto. Algunos de ellos están ampliamente tratados en otras NTP mencionadas en los correspondientes apartados.
- En este documento se revisan los principales parámetros y propiedades a considerar. Para algunos de ellos, los métodos correspondientes a su determinación cuantitativa están minuciosamente descritos en el Anexo V del Real Decreto 363/1995. En tal caso, se añade el párrafo asignado en el mismo (A1-A20).
Solubilidad en agua (A6)
Facultad o tendencia de una sustancia a mezclarse uniformemente con el agua. Generalmente, se expresa en g/100ml de agua a 20 ºC. Cuando la solubilidad no se conoce con exactitud, puede indicarse con anotaciones como: ninguna, poca, moderada, buena, muy buena. Los datos usados habitualmente para establecer el nivel de solubilidad se dan en la Tabla 5, aunque debe tenerse en cuenta que la hidrosolubilidad puede variar por la presencia de impurezas.
La solubilidad en agua es determinante en la toxicidad de una sustancia, tanto por lo que afecta a la vía de entrada como a su distribución en el organismo. También es determinante en la ecotoxicidad por cuanto afecta a la gestión de derrames y residuos (véase Ley 10/1998 de Residuos).
- TABLA 5 Criterios de solubilidad
GRADO DE SOLUBILIDAD
INTERVALO (g/100 ml de agua a 20 ºC)
Insoluble
< 0,1 g /100 ml
Poco soluble
0,1-1 g /100 ml
Moderadamente soluble
1-10 g /100 ml
Soluble
10-100 g /100 ml
Muy soluble
> 100 g /100 ml
Bienvenido al portal de riesgo químico INSHT
Portal donde
podrá encontrar la información más relevante desde el punto de vista preventivo
de esta rama de actividad.
Este portal recopila la información más
relevante contenida en la página del INSHT sobre exposición laboral a agentes
químicos y seguridad química. Incluye además diversos apartados sobre sectores
o agentes con problemática específica, almacenamiento de agentes químicos,
equipos de protección individual o información sobre el nuevo sistema
mundialmente armonizado de clasificación y etiquetado.
NTP
464: Prevención del riesgo en el laboratorio químico: operaciones básicas
NTP 508: Aseguramiento de la calidad en los laboratorios de higieneindustrial: procedimientos normalizados de trabajo (PNT)
NTP 508: Aseguramiento de la calidad en los laboratorios de higieneindustrial: procedimientos normalizados de trabajo (PNT)
Inventario
y codificación de equipos El inventario o listado (o base de datos) de los
equipos de medición disponibles debe incluir, como mínimo, los equipos
utilizados para realizar ensayos y/o calibraciones que tengan una relación
directa con los resultados, así como aquellos equipos auxiliares que requieren
de algún tipo de control, mantenimiento, verificación o calibración
Practica 2: Preparacion de disoluciones 1
Objetivo
Preparar disoluciones sencillas para habituarse a los métodos de laboratorio y su material. Las disoluciones a preparar seran las siguientes:- 500ml de cloruro de sodio de concentración 5g/l
- 100ml de cloruro de sodio de concentración 5g/l
- 250ml de cloruro de sodio de concentración 10% m/m
Recordar que al pesar se apunta la cantidad real pesada y se hace un recálculo de la concentración para poner en la etiqueta.
Laboratorio de Química
Guion del informe de las Prácticas de laboratorio:
Tiene como objetivo dar a conocer cuáles son las operaciones más comunes en el laboratorio así como sus posibilidades y, en algunos casos, las nuevas tendencias en el modo de trabajar. Paralelamente, será muy importante la adquisición, por parte del alumnado, de buenos hábitos de trabajo en el laboratorio de manera que se utilicen como pauta para poder desarrollar correctamente los experimentos prácticos que se le exigirán en cursos superiores.
- Titulo, fecha y nombre del autor.
- Objetivo de la práctica.
- Fundamento teórico.
- Materiales y reactivos.
- Precaución de seguridad.
- Procedimiento experimental.
- Observaciones y resultados experimentales.
- Conclusiones (análisis e interpretación de los resultados).
Información
- Esta publicación, enlace http://www.ub.edu/oblq/oblq%20castellano/index1.html
Tiene como objetivo dar a conocer cuáles son las operaciones más comunes en el laboratorio así como sus posibilidades y, en algunos casos, las nuevas tendencias en el modo de trabajar. Paralelamente, será muy importante la adquisición, por parte del alumnado, de buenos hábitos de trabajo en el laboratorio de manera que se utilicen como pauta para poder desarrollar correctamente los experimentos prácticos que se le exigirán en cursos superiores.
Otra faceta acerca de la seguridad en el laboratorio en la que se debe incidir es en la existencia de material a alta temperatura. La manipulación de mecheros Bunsen, agitadores con calentamiento o mantas calefactoras comporta un riesgo de quemaduras muy grande, que deben ser tratadas de inmediato ya que, en caso contrario, provocan ampollas en la piel muy molestas y que tardan muchos días en curarse. De todo lo que se ha mencionado anteriormente se deriva la necesidad de dar unos conocimientos básicos de primeros auxilios en el laboratorio, que se tienen que exponer en forma de normas concretas y de actuación rápida.
En la página web del Ministerio de Trabajo y Asuntos Sociales se encuentra información referida a la NTP 464: Prevención del riesgo en el laboratorio químico: operaciones básicas.
Enlace químico
- completar enlace con el siguiente enlace:
http://www.quimicas.net/2015/05/ejemplos-de-enlace-quimico.html
- tarea del lunes RQ
Ver el video y hacer un resumen
http://quifi-mj.blogspot.com.es/2014/05/enlace-facil-de-entender.html
copia la imagen
Cuestionarios
http://www.insht.es/portal/site/Insht/menuitem.1f1a3bc79ab34c578c2e8884060961ca/?vgnextoid=c5f044e336f1b210VgnVCM1000008130110aRCRD&vgnextchannel=9f164a7f8a651110VgnVCM100000dc0ca8c0RCRD
http://www.insht.es/portal/site/Insht/menuitem.1f1a3bc79ab34c578c2e8884060961ca/?vgnextoid=0b335cc997c84410VgnVCM1000008130110aRCRD&vgnextchannel=9f164a7f8a651110VgnVCM100000dc0ca8c0RCRD
En este apartado se incluyen varios instrumentos, en forma de cuestionarios, diseñados para facilitar la recogida sistemática y ordenada de información relativa a las condiciones de seguridad y salud en el trabajo. Los datos recopilados pueden utilizarse para completar la evaluación de riesgos, la planificación de la actividad preventiva y, en general, para la gestión de la prevención en la empresa. De forma complementaria, el uso de estos cuestionarios facilita la gestión documental de la prevención de riesgos laborales en la organización.
Identificación y prevención del riesgo en espacios confinados
Cuestionarios de promoción de la salud
Los siguientes cuestionarios, traducidos y adaptados a la realidad nacional, se ponen a disposición de las empresas como herramienta de análisis y mejora de sus actividades y como primer paso para el reconocimiento de buenas prácticas. Se presentan en dos formatos:- Como aplicación que permite la cumplimentación del cuestionario y el envío del la información para su evaluación por el INSHT, y la consiguiente respuesta sobre el resultado.
- Como archivo pdf descargable / imprimible de cuestionario completo.
http://www.insht.es/portal/site/Insht/menuitem.1f1a3bc79ab34c578c2e8884060961ca/?vgnextoid=0b335cc997c84410VgnVCM1000008130110aRCRD&vgnextchannel=9f164a7f8a651110VgnVCM100000dc0ca8c0RCRD
lunes, 3 de octubre de 2016
Exposicion del trabajo PRP2 en RFA
El viernes se expondra el trabajo
Hacer un cuestionario, 10 preguntas, para pasar al grupo
Hacer un cuestionario, 10 preguntas, para pasar al grupo
Suscribirse a:
Comentarios (Atom)